Металл
МЕТА́ЛЛЫ ─ вещества, состоящие из атомов, легко отдающих электроны в процессе химических реакций, и обладающие характерными свойствами – высокими электро- и теплопроводностью, пластичностью, положительным температурным коэффициентом электрического сопротивления, способностью хорошо отражать свет и т. д.[1]
Металл — один из элементов в китайской философской концепции Пяти первоэлементов У-син и в китайской астрологии.
Металлы как вещества[править | править код]
- Основной источник раздела: Большая российская энциклопедия[1]
К металлам относятся как собственно металлы (простые вещества), так и их сплавы и интерметаллические соединения (интерметаллиды), которые от обычных металлов отличаются более сложной кристаллической структурой. В металлическом состоянии могут находиться сильно легированные полупроводники, а также вещества, состоящие из атомов неметаллов, напр. полимерный кристалл (SN)x. Металлическими свойствами обладают также некоторые химические соединения (например, кристаллы оксидов типа MoO2, WO2, халькогенидов NbSe2, TaS2), кристаллы, содержащие органические комплексы (см. Органические проводники), многокомпонентные материалы со структурой перовскита (например, YBa2Cu3O7) или со слоистой структурой (например, Bi2Sr2CaCu2O8), являющиеся высокотемпературными сверхпроводниками.
В природе металлы существуют в составе химических соединений – оксидов, сульфидов и др., образующих руды; золото, серебро, платина, медь и др. встречаются также в самородном состоянии.
В обычных условиях металлы – твёрдые тела, имеющие кристаллическое строение (в парообразном состоянии – в основном одноатомные газы). Температуры плавления металлов выше 300 К (кроме ртути, её температура плавления –38,83 °C). Максимальную температуру плавления имеет вольфрам (около 3420 °C). При плавлении металлы сохраняют металлические свойства (см. Жидкие металлы). Искусственно созданы аморфные твёрдые металлы (см. Аморфные металлы, Стекло металлическое).
Большинство простых металлов кристаллизуется в объёмноцентрированной кубической, гранецентрированной кубической и гексагональной плотноупакованной решётках (см. Металлические кристаллы). Среди других решёток – тетрагональная с 1–2 атомами в элементарной ячейке (напр., индий). Лишь небольшое число металлов имеют более сложное строение, например низкотемпературная модификация марганца, в элементарной ячейке которого 58 атомов. Многие металлы в зависимости от температуры и давления могут существовать в различных кристаллических модификациях. Некоторые вещества в зависимости от кристаллической структуры могут быть металлами, диэлектриками, полупроводниками или полуметаллами, например олово (белое олово с тетрагональной структурой – металл, серое олово с кубической структурой алмаза – полупроводник), углерод (графит – полуметалл, алмаз – диэлектрик) (см. Полиморфизм).
Металлы и сплавы обычно состоят из большого числа мелких кристаллов (зёрен), неразличимых невооружённым глазом. Зёрна могут иметь округлую или вытянутую форму, быть крупными или мелкими и располагаться относительно друг друга в определённом порядке или случайно. Форма, размер и взаимное расположение, а также ориентировка зёрен зависят от условий их образования.
Историческая справка[править | править код]
Термин «металл» произошёл от греческого слова μέταλλον (от μεταλλεύω – выкапывать, добывать из земли), которое первоначально означало «копи, рудники» (в этом значении оно встречается у Геродота в 5 в. до н. э.). То, что добывалось в рудниках, Платон называл μεταλλεία . В древности и в средние века считалось, что существует только 7 металлов: золото, серебро, железо, ртуть, олово, медь, свинец. По алхимическим представлениям, металлы зарождались в земных недрах под влиянием «лучей» планет и постепенно совершенствовались, превращаясь в золото (см. Алхимия). Алхимики полагали, что металлы – вещества сложные, состоящие из «начала металличности» (ртути) и «начала горючести» (серы). В начале 18 века получила распространение гипотеза, согласно которой неблагородные металлы состоят из золы («окалины») и «начала горючести» – флогистона. М. В. Ломоносов насчитывал 6 металлов (золото, серебро, медь, олово, железо, свинец) и определял меьаллы как «светлое тело, которое ковать можно». В конце 18 века А. Лавуазье опроверг гипотезу флогистона. В руководстве по химии (1789) он дал список простых веществ, 17 из которых отнёс к металлам (сурьма, серебро, мышьяк, висмут, углерод, медь, олово, железо, марганец, ртуть, молибден, никель, золото, платина, свинец, вольфрам, цинк). По мере развития методов химического исследования число известных металлов возрастало. В 1-й половине 19 века были открыты спутники платины, получены путём электролиза некоторые щелочные и щёлочноземельные металлы, положено начало разделению редкоземельных металлов, при химическом анализе минералов открыты неизвестные ранее металлы. В 1860–63 методом спектрального анализа открыты цезий, рубидий, таллий, индий. В конце 19 – начале 20 веков подтвердилось существование металлов, предсказанных Д. И. Менделеевым на основе периодического закона. Открытие радиоактивности в конце 19 века повлекло за собой поиски природных радиоактивных металлов. Начиная с 1930–1940-х гг. методом ядерных превращений искусственно получены радиоактивные металлы, в частности трансурановые элементы.
Широкое использование металлов привело к тому, что их основные физические свойства были изучены ещё в 19 веке. Микроскопическая теория металлов начала развиваться в 20 веке. В 1900 П. Друде предложил модель металла, в которой электропроводность осуществляется потоком электронного газа, заполняющего промежутки между атомами. Х. Лоренц развил идею Друде, применив к электронному газу кинетическую теорию газов. Однако построенная на применении законов классической механики и статистики теория Друде – Лоренца не могла объяснить некоторые экспериментальные факты. В 1927–28 В. Паули и А. Зоммерфельд устранили ряд недостатков теории Друде, предположив, что основная часть электронного газа в металлах при обычных температурах находится в вырожденном состоянии; эти работы легли в основу современной электронной теории металлов.
В 1929–30 Ф. Блох и Л. Бриллюэн рассмотрели влияние периодического поля кристаллической решётки на электронный газ, что привело к созданию зонной теории твёрдых тел. Применение к электронам в металлах теории обменного взаимодействия (В. Гейзенберг, П. Дирак, 1928) позволило понять природу ферромагнетизма и обнаружить новые магнитоупорядоченные состояния металлов – антиферромагнетизм (Л. Неель, 1932) и ферримагнетизм. В 1911 Х. Камерлинг-Оннес открыл явление сверхпроводимости. Исследование взаимодействия электронов друг с другом и с решёткой позволило раскрыть природу этого явления (Дж. Бардин, Л. Купер, Дж. Шриффер, 1956). Изучение нормальных, сверхпроводящих и магнитоупорядоченных металлов – три основных направления современной микроскопической теории металлов.
Химические свойства и методы получения[править | править код]
В длинной форме периодической системы химических элементов граница между элементами-металлами и элементами-неметаллами проводится по диагонали от бора до астата: металлы расположены слева от этой линии (к металлам относятся около 90 известных химических элементов, точнее – все элементы за исключением водорода, бора, углерода, кремния, азота, фосфора, мышьяка, кислорода, серы, селена, теллура, галогенов и благородных газов). По строению атома металлы подразделяются на непереходные и переходные; среди непереходных металлов выделяют щелочные и щёлочноземельные, среди переходных – d- и f-металлы, а также редкоземельные, платиновые, трансурановые и др. металлы (см. в статье Химические элементы).
Для атомов металлов характерны более низкие значения энергии ионизации, чем для атомов неметаллов. В изменении значений энергии ионизации атомов металлов при увеличении их порядкового номера явно выражена периодичность: в общем, при увеличении порядкового номера в пределах отдельного периода энергии ионизации металлов возрастают, при увеличении порядкового номера в пределах отдельной группы – убывают; отклонения от этой тенденции обусловлены строением электронных оболочек атомов (подробнее см. в статье Периодическая система химических элементов).
Слабой связью валентных электронов с ядром атома объясняются многие свойства металлов, проявляющиеся в химических процессах: образование положительно заряженных ионов (катионов), образование осно́вных оксидов и гидроксидов с осно́вными свойствами (оснований), замещение водорода в кислотах и т. д. В химических реакциях металлы выступают как доноры электронов (восстановители); в кристаллах химических соединений с другими элементами, а также в водных растворах соединений образуют в основном элементарные катионы (в растворах – аквакатионы). Металлы могут входить в состав сложных анионов, например перманганат-анион MnO4−, в т. ч. комплексных, например ацидокомплекс [Fe(CN)6]4–. В сложных ионах и полярных молекулах атомы металлов являются центрами положительного заряда. Способность образовывать отрицательно заряженные элементарные ионы для металлов нехарактерна (тем не менее формально отрицательные степени окисления металлов встречаются в целом ряде комплексных соединений).
Наиболее распространённая химическая реакция, свойственная всем металлам, – окисление. Способность металлов к окислению меняется в очень широких пределах. Многие металлы окисляются кислородом воздуха уже при комнатной температуре, однако скорость и механизм реакции очень сильно зависят от природы металла. Большинство металлов при взаимодействии с кислородом образуют оксиды, щелочные (кроме лития) и щёлочноземельные металлы – также пepоксиды и надпероксиды. Окисление приводит к формированию на поверхности компактного металла плёнки оксида. Такие плёнки, как правило, имеют рыхлую структуру, и их образование не защищает металл от дальнейшего окисления. Очень плотные плёнки, предохраняющие металл от дальнейшего окисления, характерны, например, для алюминия, титана, хрома, которые устойчивы на воздухе, хотя и обладают высокой химической активностью. Крайне неустойчивы на воздухе щелочные металлы. С азотом ряд металлов (например, литий) реагируют при комнатной температуре, другие металлы (например, магний, цирконий, гафний, титан) – при нагревании; при этом образуются нитриды. Многие металлы активно взаимодействуют с водородом (образуются гидриды), галогенами (галогениды), серой (сульфиды), фосфором (фосфиды), другими неметаллами. Наиболее активные металлы реагируют с углеродом, образуя карбиды и ацетилениды. В результате металлирования органических молекул образуются металлоорганические соединения. При сплавлении металлов друг с другом – твёрдые растворы или интерметаллиды.
Металлы, имеющие переменную валентность (например, хром, марганец, железо), в соединениях, отвечающих низшим степеням окисления (Cr2+, Mn2+, Fe2+), проявляют восстановительные свойства; в высших степенях окисления те же металлы (Cr6+, Mn7+, Fe3+) обнаруживают окислительные свойства. Для водных растворов и растворов электролитов окислительно-восстановительные свойства металлов выражают с помощью электрохимического ряда напряжений (см. в статье Электродный потенциал). Металлы, для которых стандартные электродные потенциалы меньше, чем –0,413 В, окисляются водой с выделением H2 (щелочные и щёлочноземельные металлы реагируют с водой при комнатной температуре; такие металлы, как цинк или железы, реагируют с водяным паром при высоких температурах). С растворами щелочей взаимодействуют металлы, образующие растворимые анионные гидроксокомплексы (бериллий, цинк, алюминий, галлий, олово). Большинство металлов окисляются теми или иными кислотами. Металлы, стоящие в электрохимическом ряду напряжений до водорода, окисляются ионами H+ и поэтому растворяются при действии неокисляющих кислот (HCl или разбавленной H2SO4), но только если не образуются нерастворимые продукты; реакции способствует образование анионных комплексов. Азотная кислота, даже разбавленная, окисляет многие металлы. При этом, если ионы металлов устойчивы в низших степенях окисления, образуются катионные комплексы, если в высших, как в случае, например, рения, – анионные (ReO4−). Некоторые металлы реагируют с разбавленными HNO3 и H2SO4 с образованием катионных комплексов и пассивируются в концентрированных растворах этих кислот. Для растворения малоактивных металлов, например золота или платины, используют смеси, содержащие окислитель и донор лигандов, необходимый для образования растворимых комплексов (например, смеси HNO3 с HCl или HNO3 с HF).
Важная характеристика металлов – их способность образовывать осно́вные оксиды и соответствующие гидроксиды, а также соли – продукты замещения в кислотах протона на ион металла. На примере гидроксидов металлов можно проследить закономерности изменения свойств соединений в зависимости от изменения металлического характера элемента; в частности, наиболее типичные металлы – щелочные – образуют наиболее сильные основания (см. в статье Щёлочи). О взаимодействии металлов со средой, ведущей к их разрушению, см. в статье Коррозия.
Для получения металлов практическое значение имеют несколько основных методов: восстановление оксидов металлов углеродом или водородом; восстановление оксидов металлов другими металлом (металлотермия); восстановление галогенидов или сульфидов металлов водородом или металлами; термическое разложение подходящих соединений металлов (например, карбонилов); электрохимические методы. Поскольку достижению требуемых эксплуатационных характеристик мешает присутствие в металлах примесей, используются различные методы очистки металлов (зонная плавка, экстракционные методы и т.д.).
Подробнее о свойствах, методах получения и очистки металлов можно узнать в статьях, посвящённых отдельным металлам или их группам. См. также Металловедение, Металлургия.
Металлическое состояние[править | править код]
Металлы можно представить как вещества, состоящие из положительных ионов и свободных электронов (электронов проводимости). Электроны компенсируют силы отталкивания, действующие между положительно заряженными ионами, и тем самым способствуют связыванию их в твёрдое тело или жидкость (металлическая связь, см. в статье Химическая связь). Электроны проводимости определяют электрические, магнитные, оптические свойства металлов, а также их теплопроводность, а при низких температурах – теплоёмкость. Значительна роль электронов в сжимаемости металлов и других механических свойствах; их наличие делает металлы пластичными. Изменение электронного спектра иногда служит причиной фазовых переходов в металлах, при которых изменение кристаллической структуры носит вторичный характер (например, переход из нормального состояния металлов в сверхпроводящее или из парамагнитного в ферро- или антиферромагнитное).
Важнейшая характеристика металлического состояния – число электронов проводимости [math]\displaystyle{ n }[/math] в 1 см3 (или их число на элементарную ячейку кристалла либо на 1 атом). Как правило, из всех электронов атома коллективизируются только валентные. Это даёт возможность по химическим свойствам атомов, из которых состоит кристалл, и по его геометрической структуре определить [math]\displaystyle{ n=Z/V_0 }[/math], где [math]\displaystyle{ Z }[/math] – число валентных электронов, [math]\displaystyle{ V_0 }[/math] – объём элементарной ячейки.
Многие свойства металлов можно объяснить, считая, что электроны проводимости – идеальный вырожденный газ фермионов, а роль ионов сводится к созданию потенциальной ямы, в которой движутся электроны (модель Друде – Лоренца – Зоммерфельда; см. Теория Друде, Теория Зоммерфельда). В этой модели температура вырождения [math]\displaystyle{ T_ \mathrm{F} }[/math] электронного газа порядка 104–105 К, то есть практически при любой температуре существования металлов электронный газ в нём вырожден (см. Вырожденный газ).
Более полное объяснение свойств металлов даёт зонная теория твёрдого тела, которая рассматривает движение отдельных электрона в периодическом поле с потенциалом [math]\displaystyle{ U_ \boldsymbol{(r)} }[/math], создаваемом ионами кристаллической решётки и остальными электронами (одноэлектронное приближение): [math]\displaystyle{ U( \boldsymbol r+a)=U_\boldsymbol{(r)} }[/math], где [math]\displaystyle{ \boldsymbol r }[/math] – пространственная координата точки, [math]\displaystyle{ \boldsymbol a }[/math] – период решётки (см. Блоховские электроны).
Периодичность [math]\displaystyle{ U_{\boldsymbol {(r)}} }[/math] позволяет характеризовать стационарное состояние электрона проводимости квазиимпульсом [math]\displaystyle{ \boldsymbol p=\boldsymbol{ℏk} }[/math] ([math]\displaystyle{ \boldsymbol ℏ }[/math] – постоянная Планка, [math]\displaystyle{ \boldsymbol k }[/math] – квазиволновой вектор), аналогичным импульсу частицы в свободном пространстве. Волновая функция электрона в стационарном состоянии – решение уравнения Шрёдингера для электрона, отвечающее собственному значению энергии электрона [math]\displaystyle{ \mathcal E_s }[/math]. Волновая функция и собственное значение энергии (в отличие от случая свободного электрона) – периодические функции квазиимпульса. Индекс s, нумерующий решения уравнения Шрёдингера, называют номером зоны, [math]\displaystyle{ \mathcal E_s( \mathbf{p}) }[/math] – законом дисперсии электронов или электронным спектром кристалла, соответствующим полю. В каждой разрешённой энергетической зоне состояния электронов заполняют полосу между [math]\displaystyle{ \mathcal E_{мин} }[/math] и [math]\displaystyle{ \mathcal E_{макс} }[/math]. Зоны могут перекрываться, но их индивидуальность при этом сохраняется. С помощью законов дисперсии можно рассчитать плотность электронных состояний в энергетической зоне.
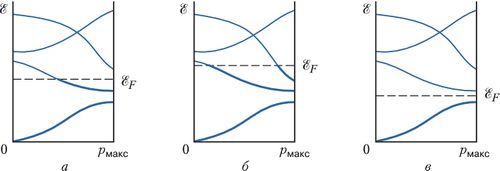
Зонный характер спектра и Паули принцип позволяют сформулировать принципиальное отличие металлов от диэлектрика. Tак как в каждую зону может «поместиться» не более [math]\displaystyle{ 2N }[/math] электронов ([math]\displaystyle{ N }[/math] – число атомов в кристалле), то в зависимости от числа электронов, приходящихся на 1 атом, и взаимного расположения зон могут осуществляться два случая: либо в основном состоянии (при [math]\displaystyle{ T=0 К }[/math]) имеются зоны, частично заполненные электронами (рис. а, б), либо есть только целиком заполненные зоны и пустые (рис. в). В первом случае кристалл является металлом (рис. б соответствует полуметаллу), во втором – диэлектриком (или полупроводником).
В металлах граница заполнения уровней электронами (энергия Ферми [math]\displaystyle{ \mathcal E_F }[/math]) попадает в разрешённую зону. Соответствующая ей изоэнергетическая поверхность [math]\displaystyle{ \mathcal E({\bf p})=\mathcal E_F }[/math] (поверхность Ферми) отделяет область занятых электронами состояний от свободных в импульсном пространстве.
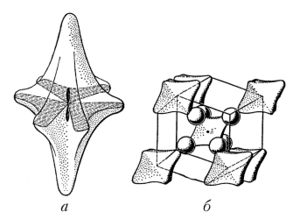
Поверхности Ферми щелочных металлов (литий, натрий, калий, рубидий, цезий) – почти идеальные сферы. Это не означает, что электроны этих металлов не испытывают влияния ионов. Их эффективные массы отличаются от массы свободного электрона [math]\displaystyle{ m_0 }[/math], например у натрия [math]\displaystyle{ m=1,24m_0 }[/math]. У всех металлов, кроме перечисленных, поверхности Ферми имеют сложную форму.
Некоторые свойства металлов (главным образом в сильном магнитном поле) очень чувствительны к форме поверхности Ферми (см. эффект Де Хааза – ван Альвена, эффект Шубникова – де Хааза), что позволило экспериментально определить поверхность Ферми многих металлов и интерметаллических соединений.
Методы зонной теории позволили определить законы дисперсии, выяснить происхождение отдельных характерных деталей электронного спектра металлов. При всей сложности законов дисперсии представление об электронах металлов как лёгких (по сравнению с ионами) заряженных частицах является правильным на качественном уровне и позволяет в рамках модели Друде – Лоренца – Зоммерфельда оценить порядок величин основных характеристик металлов – электронной теплоёмкости, электро- и теплопроводности, толщины скин-слоя (см. Скин-эффект) и т. п. У некоторых соединений (CeAl3, CeCu6, CeCu2Si2, UB13 и др.) обнаружены необычные свойства (например, гигантская электронная теплоёмкость), указывающие на то, что в них есть электроны, обладающие аномально большой эффективной массой.
При высоких давлениях, когда объём, приходящийся на 1 атом, уменьшается, атомы теряют свою индивидуальность и любое вещество превращается в сильно сжатую электронно-ядерную плазму, то есть в своеобразный металл. Металлизация любого вещества происходит при плотности [math]\displaystyle{ ≫20Z^2 }[/math], где [math]\displaystyle{ Z }[/math] – атомный номер вещества. При таких плотностях большинство свойств вещества определяется вырожденным электронным газом.
Электрические свойства[править | править код]
При комнатной температуре удельная электрическая проводимость [math]\displaystyle{ σ }[/math] металлов порядка 10–8–10–6 Ом–1•м–1; с понижением температуры она увеличивается. Характерное свойство металлов в нормальном (несверхпроводящем) состоянии – линейная зависимость между плотностью тока [math]\displaystyle{ j }[/math] и напряжённостью [math]\displaystyle{ E }[/math] приложенного электрического поля (закон Ома): [math]\displaystyle{ j=σE }[/math].
Носители тока в металлах – электроны проводимости с энергией, близкой к [math]\displaystyle{ \mathcal E_F }[/math]. Причина электрического сопротивления – рассеяние электронов на любых нарушениях периодичности кристаллической решётки: тепловых колебаниях ионов (фононах), самих электронах, а также различных дефектах – примесных атомах, вакансиях, дислокациях, границах кристаллов и образца (см. Рассеяние носителей заряда). Мерой рассеяния служит длина свободного пробега [math]\displaystyle{ l }[/math] – среднее расстояние между двумя последовательными столкновениями электронов с дефектами:
где [math]\displaystyle{ n }[/math] – концентрация электронов проводимости (порядка 1022–1023 см–3), [math]\displaystyle{ e }[/math] – заряд электрона, [math]\displaystyle{ p_F=2πℏ(3n/8π)^{1/3} }[/math] – так называемый граничный фермиевский импульс. При [math]\displaystyle{ T=300 К }[/math] длина свободного пробега [math]\displaystyle{ l }[/math] порядка 10–6 см; с понижением [math]\displaystyle{ T }[/math] длина пробега растёт, достигая (для высококачественных монокристаллических образцов) 0,1–1 см. Соответственно возрастает электрическая проводимость [math]\displaystyle{ σ }[/math] и уменьшается удельное электрическое сопротивление [math]\displaystyle{ ρ=σ–1 }[/math]. Отношение проводимости при [math]\displaystyle{ T=4,2 К }[/math] к проводимости при [math]\displaystyle{ T=300 К }[/math] характеризует совершенство и химическую чистоту металлов.
Сопротивление сплавов значительно выше сопротивления чистых металлов. Причина этого в нарушении идеальности кристаллической решётки (различные атомы в узлах решётки) и наличии дефектов. В веществах с большим [math]\displaystyle{ ρ }[/math] возникает локализация электронных состояний – проводимость исчезает (см. Андерсоновская локализация).
При плавлении металлов подвижные электроны в нём сохраняются, поэтому сохраняется и большая электрическая проводимость, хотя разрушение дальнего порядка приводит к скачкообразному росту сопротивления [math]\displaystyle{ ρ }[/math]. Исключение составляют сурьма, галлий, висмут, электрическое сопротивление которых при плавлении уменьшается. При [math]\displaystyle{ T→0 К }[/math] у большинства металлов происходит исчезновение электрического сопротивления – они переходят в сверхпроводящее состояние.
Тепловые свойства[править | править код]
Теплоёмкость металлов обусловлена ионным остовом (решёточная теплоёмкость [math]\displaystyle{ C_p }[/math]) и электронным газом (электронная теплоёмкость [math]\displaystyle{ C_э }[/math]). Хотя концентрация электронов проводимости в металлах велика и не зависит от температуры, [math]\displaystyle{ C_э }[/math] наблюдается у большинства металлов только при низких температурах (порядка нескольких [math]\displaystyle{ K }[/math]), так как электронный газ в металлах вырожден. При уменьшении температуры [math]\displaystyle{ C_p }[/math] убывает пропорционально [math]\displaystyle{ T^3 }[/math], а [math]\displaystyle{ C_э }[/math] – пропорционально [math]\displaystyle{ T }[/math]. Электроны проводимости вносят линейный по [math]\displaystyle{ T }[/math] вклад и в коэффициент теплового расширения металлов.
Электроны проводимости принимают участие не только в переносе электрического заряда, но и в переносе теплоты. Вследствие большой подвижности электронов проводимости теплопроводность металлов велика. Удельная электропроводность и электронная часть теплопроводности металлов связаны соотношением, называемым законом Видемана – Франца. Теплопроводность сплавов ниже теплопроводности чистых металлов.
При наличии градиента температуры в металле возникает электрический ток или разность потенциалов (термоэдс). Из-за вырождения электронного газа коэффициенты, описывающие термоэдс и другие термоэлектрические эффекты, малы, однако их исследование позволяет обнаружить увлечение электронов тепловыми фононами. Взаимодействие возбуждённых в металле акустических волн с электронами проводимости приводит к возникновению электрического тока либо разности потенциалов, пропорциональной интенсивности потока фононов (см. Акустоэлектрический эффект).
Магнитные свойства[править | править код]
Электроны проводимости обладают как парамагнитными (из-за наличия у каждого электрона собственного магнитного момента), так и диамагнитными (связанными с квантованием движения электронов в плоскости, перпендикулярной магнитному полю) свойствами (см. Парамагнетизм, Диамагнетизм). В магнитную восприимчивость металлов вносят вклад и ионы: у непереходных металлов ионы диамагнитны, у переходных, как правило, парамагнитны. Из-за вырождения электронного газа парамагнитная восприимчивость [math]\displaystyle{ χ }[/math] электронного газа слабо зависит от [math]\displaystyle{ T }[/math] (см. парамагнетизм Паули). При низких температурах и в сильных магнитных полях напряжённостью [math]\displaystyle{ H }[/math] парамагнитная восприимчивость [math]\displaystyle{ χ }[/math] металлических монокристаллов осциллирует как функция [math]\displaystyle{ 1/H }[/math] (эффект де Хааза – ван Альвена).
Все переходные металлы с недостроенными d- или f-электронными оболочками – парамагнетики. Некоторые металлы при понижении температуры переходят в магнитоупорядоченное состояние: ферромагнитное (например, железо, кобальт, никель, гадолиний), антиферромагнитное (например, цезий, марганец) или в состояние с геликоидальной магнитной атомной структурой (например, хром). При этом электроны проводимости играют существенную роль в формировании магнитных структур (см. Ферромагнетизм, Антиферромагнетизм). Большинство непереходных металлов остаются парамагнетиками или диамагнетиками вплоть до [math]\displaystyle{ T=0 К }[/math]. Магнитное упорядочение существенно влияет на все другие свойства металлов, в частности на электрические свойства – в электрическое сопротивление вносит вклад рассеяние электронов на спиновых волнах.
Переход металлов в сверхпроводящее состояние сопровождается изменением его магнитных свойств: в сверхпроводящем состоянии в слабых полях металл проявляет себя как диамагнетик, в котором магнитное поле равно нулю из-за экранирования внешнего магнитного поля незатухающими вихревыми токами (см. эффект Мейснера). В сверхпроводниках 1-го рода (олово, свинец, индий и др.) это выполняется вплоть до полей, разрушающих сверхпроводимость. В сверхпроводниках 2-го рода (Nb3Sn, NbTi и др.) магнитное поле в широком диапазоне напряжённостей [math]\displaystyle{ H }[/math], не разрушая сверхпроводимость, проникает в объём металла в виде вихрей, что ослабляет диамагнетизм.
Гальваномагнитные и термомагнитные явления[править | править код]
Если металлический образец, по которому течёт электрический ток, поместить в постоянное магнитное поле, то в нём возникают явления, обусловленные искривлением траекторий электронов в плоскости, перпендикулярной [math]\displaystyle{ H }[/math], что приводит к изменению кинетических коэффициентов (коэффициент электро- и теплопроводности, термоэлектрический коэффициент и др.) и к ряду новых явлений: эффекту Холла, магнитосопротивлению и др. На зависимость кинетических коэффициентов от [math]\displaystyle{ H }[/math] влияют особенности электронного энергетического спектра металла, в частности топология поверхности Ферми (см. Гальваномагнитные явления, Термогальваномагнитные явления). Даже не слишком сильное магнитное поле при низких температурах (порядка 1К) может изменить кинетические свойства металла, например в десятки тысяч раз увеличить поперечное (относительно направления [math]\displaystyle{ H }[/math]) сопротивление (у висмута) или практически полностью «выключить» поперечную электронную теплопроводность металла.
Эмиссия электронов[править | править код]
При нагревании металлов до высоких температур наблюдается эмиссия («испарение») электронов с поверхности металла (см. Термоэлектронная эмиссия). Число электронов, вылетающих из металла в единицу времени, пропорционально [math]\displaystyle{ ехр(–W/kT) }[/math], где [math]\displaystyle{ W }[/math] – работа выхода электрона из металла, [math]\displaystyle{ k }[/math] – постоянная Больцмана. Величина [math]\displaystyle{ W }[/math] у различных металлов (и даже на разных кристаллических гранях одного металла) различна и составляет 2–5 эВ; [math]\displaystyle{ W }[/math] зависит от состояния поверхности. Различия в [math]\displaystyle{ W }[/math] обусловливают контактную разность потенциалов между различными металлами. Эмиссия электронов с поверхности металла происходит также в сильных электрических полях (напряжённостью порядка 107 В/см) в результате туннельного прохождения электронов через сниженный полем потенциальный барьер (см. Автоэлектронная эмиссия). Туннелирование электронов через малый (меньше 1 нм) зазор лежит в основе сканирующей туннельной микроскопии.
Эмиссия электронов возникает также под действием электромагнитного излучения видимого и УФ-диапазонов – фотоэлектронная эмиссия, при бомбардировке поверхности металла электронами – вторичная электронная эмиссия, или ионами – ионно-электронная эмиссия, при взаимодействии поверхности металла с плазмой – взрывная электронная эмиссия.
Металлы в электромагнитных полях[править | править код]
Переменный электрический ток частоты [math]\displaystyle{ ω }[/math] течёт по поверхности металла, проникая в него на глубину скин-слоя толщиной [math]\displaystyle{ δ=c\sqrt{2πσω} }[/math], где [math]\displaystyle{ c }[/math] – скорость света (см. Высокочастотная проводимость); например, для Cu [math]\displaystyle{ δ≈6·10^{–6} }[/math] м при [math]\displaystyle{ ω=6·10^{–8} }[/math] Гц. При падении электромагнитной волны на поверхность металда часть электромагнитной энергии поглощается в скин-слое, а другая часть переизлучается электронами и отражается от поверхности металла. Коэффициент отражения для Cu≈2·10{–5}.
При падении на металл, помещённый в сильное постоянное магнитное поле, электромагнитных волн, частота которых равна или кратна циклотронной частоте электронов проводимости, в металле наблюдаются резонансные явления (см. Циклотронный резонанс). В некоторых металлах (например, щелочных) можно наблюдать электронный парамагнитный резонанс на электронах проводимости и спиновые волны.
Металлы, помещённый в достаточно сильное магнитное поле при низкой температуре, обладает многими свойствами, характерными для плазмы: в нём могут распространяться разнообразные слабозатухающие волны (геликоны, магнитоплазменные волны, доплероны и др.) (см. Плазма твёрдых тел).
Оптические свойства[править | править код]
Для электромагнитных волн оптического диапазона металлы, как правило, непрозрачны. Характерный блеск – следствие практически полного отражения света поверхностью металла. При взаимодействии света с электронами проводимости металлов важную роль играет внутренний фотоэффект, то есть вынужденные (за счёт поглощения фотонов) переходы электронов из одной энергетической зоны в другую. Как правило, именно внутренний фотоэффект определяет коэффициент поглощения излучения видимого и ультрафиолетового диапазонов и изменение проводимости металла под воздействием света (см. Фотопроводимость). Чем выше частота излучения, тем меньшую роль играют электроны проводимости во взаимодействии излучения с металлом: в ультрафиолетовом и рентгеновском диапазонах оптические свойства металлов мало отличаются от свойств диэлектриков.
Отражение плоскополяризованного света от поверхности металла сопровождается поворотом плоскости поляризации и появлением эллиптической поляризации. Это явление используется для технических целей и для определения оптических констант металла. См. также Металлооптика.
Механические свойства[править | править код]
Для металлов характерно сочетание высокой пластичности и высокой вязкости со значительными прочностью, твёрдостью и упругостью. Соотношение этих свойств можно регулировать с помощью механической и термической обработки металлов, а в сплавах – изменением концентрации компонентов. Упругая деформация металлов и их сплавов находится в пределах 0,01–1%, пластическая – много больше и при комнатной температуре может достигать 10–100%.
Сопротивление изотропного поликристаллического металла воздействию внешних механических сил описывают в зависимости от типа деформации (растяжение, сдвиг, объёмное сжатие) различными модулями упругости (модулями Юнга [math]\displaystyle{ E }[/math], сдвига [math]\displaystyle{ G }[/math] и объёмного сжатия [math]\displaystyle{ K }[/math] соответственно), между которыми существует линейная связь через коэффициент Пуассона [math]\displaystyle{ ν }[/math]: [math]\displaystyle{ E=3K(1−2ν) }[/math]; [math]\displaystyle{ E=G[2(1+ν)] }[/math]. Для большинства металлов [math]\displaystyle{ ν }[/math] находится в пределах 0,22-0,46. Модули упругости металлов определяются межатомными взаимодействиями. В монокристалле модули упругости зависят от направления, поэтому они образуют тензор. Величина модуля сдвига [math]\displaystyle{ G }[/math] металла лежит в пределах от 0,39 ГПа (цезий) до 224 ГПа (осмий), у железа [math]\displaystyle{ G=84,1 }[/math] ГПа. При увеличении температуры модули упругости монотонно убывают; изменение модуля упругости в интервале от [math]\displaystyle{ 0 К }[/math] до температуры плавления составляет около 50% от исходного значения. В области упругого поведения в металле возможно проявление внутреннего трения.
Пластическая деформация металла осуществляется относительным сдвигом (скольжением) параллельных атомных плоскостей. Теоретически сопротивление металлов пластической деформации и разрушению составляет [math]\displaystyle{ 10^{–1}G }[/math] (одновременный разрыв всех связей в плоскости скольжения). Экспериментально пластическая деформация и разрушение наблюдаются при напряжениях [math]\displaystyle{ 10^{–4}–10^{–2}G }[/math]. Это различие обусловлено существованием носителей пластической деформации – дислокаций – линий, вдоль которых происходит разрыв связей. Движение дислокаций вдоль определённых плоскостей в кристалле обеспечивает сдвиг одной части кристалла относительно другой. Прочность и пластичность металла обусловлены движением и взаимодействием дислокаций между собой и с другими дефектами, примесями и их скоплениями, границами раздела фаз, включениями других фаз.
Механические характеристики металла можно изменять в широких пределах термической и механической обработкой, а также введением примесей (легированием). Например, предел прочности железа (технической чистоты) 0,35 ГПа, тогда как высокопрочные легированные стали (сплавы железа с другими металлами и с углеродом) имеют предел прочности от 1,5 до 4,5 ГПа.
Применение металлов[править | править код]
В технике в основном применяют сплавы металлов. Так, например, из-за малой прочности чистые металлы непригодны в качестве материалов для изготовления конструкций, но многие сплавы металлов обладают одновременно высокой механической прочностью и высокой пластичностью и находят широкое применение в качестве конструкционных материалов. Металлы с низким уровнем внутреннего трения, слабо рассеивающие энергию колебаний, используют при изготовлении акустических резонаторов музыкальных инструментов. Металлы и их сплавы используют: в электротехнике как в качестве проводников электрического тока (медь, алюминий), так и в качестве материалов для резисторов и электронагревательных элементов (нихром и т. п.); в инструментальной технике для изготовления рабочей части инструментов (в основном это инструментальные стали и твёрдые сплавы).
Литература статьи Большой российской энциклопедии[править | править код]
- Абрикосов А. А. Основы теории металлов. 2-е изд. M., 2009.
- Бернштейн M. Л., Займовский В. А. Механические свойства металлов. 2-е изд. M., 1979.
- Гринвуд Н., Эрншо А. Химия элементов. М., 2008. Т. 1–2.
- Зайцев Б. Е. Общие физические и химические свойства металлов. М., 1987.
- Редкие и рассеянные элементы: Химия и технология / Под ред. С. С. Коровина. М., 1996–2003. Т. 1–3.
- Штремель М. А. Прочность сплавов. М., 1982–1997. Ч. 1–2.
Металл в китайской астрологии и китайской медицине[править | править код]
- Источник раздела: Новая астрологическая энциклопедия[2]
- Основная статья: У-син (пять первоэлементов)
Металл в китайской астрологии — одна из пяти стихий (у син).
Металл связывается с планетой Венера, западом, осенью (30 августа - 11 ноября по григорианскому календарю), белым цветом, терпким вкусом и прогорклым запахом, числом 9, земными "ветвями" обезьяны (шэнь) и петуха (ю), 7-м и 8-м небесными "стволами" (гэн, синь; в том числе соотносится с годами, оканчивающимися на 0 и 1), с ци (энергией) сухости, в организме человека — с лёгкими и толстой кишкой. В цикле пяти стихий металл символизирует достигнутую прочность и падение активности. Металл связан с заботами и справедливостью; с носом, кожей, волосами на теле.
Старинные китайские источники гласят: когда правит стихия металл, император не должен разрешать взрывать скалы и рыть шахты, в противном случае его войска будут разбиты, воины погибнут, а он сам потеряет трон.
Металл связан с западной ци (энергией) сухости, "двигающей" сезон осени. Действие этой ци ощущается с 23 сентября по 3 декабря. Родившиеся под влиянием металла чувствуют своё призвание в служении истине и красоте. Главное для них — оставаться верными самим себе, не отрекаясь от своей натуры, обогащать повседневность произведениями искусства и культуры. Лучше исправлять жизненные условия окружающих, чем преследовать эгоистические цели.
Литература статьи Новой астрологической энциклопедии[править | править код]
- Александер Китайская астрология.
- Жэнь Инцю Базовая теория китайской медицины: Пять вращений, шесть энергий.
- Китайская философия.
- Элис Р. Китайская астрология.// О чём говорит год рождения. Восточные гороскопы.
Примечания[править | править код]
Пальпация : Пульсовая диагностика • Пальпация конечностей • Пальпация груди • Пальпация живота • Пальпация точек
Диагностика по звукам • Диагностика по запахам