Паркинсонизм
- Основной источник статьи: Болезни нервной системы[1]
Паркинсонизм — синдром, характеризующийся любым сочетанием гипокинезии с ригидностью, тремором (преимущественно покоя) и постуральной неустойчивостью. Наиболее частой формой синдрома паркинсонизма является идиопатический паркинсонизм, или болезнь Паркинсона. Кроме того, ряд случаев приходится на вторичный паркинсонизм, развитие которого связано с воздействием определенного этиологического фактора. Паркинсонизм может быть одним из основных или дополнительных проявлений других дегенеративных заболеваний с поражением экстрапирамидной системы.
Исторические аспекты[править | править код]
Болезнь Паркинсона впервые описал английский врач Джеймс Паркинсон в 1817 году в своем «Эссе о дрожательном параличе», в котором обобщил результаты наблюдений за шестью пациентами.
В 1817 г. английский врач Джеймс Паркинсон описал заболевание, основным проявлением которого были общая скованность и дрожание, и назвал его «shaking palsy» (дрожательный паралич).
На основе наблюдений за шесть пациентами им было написано «Эссе о дрожательном параличе».[2][3]
Латинским эквивалентом является термин «paralisis agitans».
Дж. Паркинсон описывал следующие характерными проявлениями заболевания:[2][3]
- непроизвольные дрожательные движения
- ослабление мышечной силы
- ограничение активности движений
- туловище больного наклонено вперед
- ходьба переходит в бег
- при перечисленных симптомах чувствительность и интеллект больного остаются сохранными.
В 1877 г. Шарко дал более подробное описание клинических симптомов заболевания и предложил название — «болезнь Паркинсона». Когда в начале XX в. выяснилось, что симптомы, типичные для болезни Паркинсона, могут развиваться вследствие различных причин, возник термин «синдром паркинсонизма».
Классификация паркинсонизма[править | править код]
- Болезнь Паркинсона (идиопатический паркинсонизм, первичный паркинсонизм).
- Вторичный паркинсонизм (симптоматический):
- лекарственный (нейролептики, препараты раувольфии, а-метилдофа, антагонисты кальция, препараты лития, ингибиторы обратного захвата серотонина и др.);
- токсический (МФТП, марганец, окись углерода, сероуглерод, цианиды, метанол, фосфорорганические соединения, нефтепродукты и др.);
- постгипоксический (двусторонний некроз бледного шара);
- энцефалитический (прогрессирующие последствия летаргического энцефалита Экономо, в острой стадии вирусных энцефалитов с последующим регрессом, при СПИДе, нейроборрелиозе и др.);
- травматический (тяжелые ЧМТ, энцефалопатия боксеров);
- при объемных процессах (опухоль, абсцесс, гумма, туберкулома в области базальных ганглиев или черной субстанции);
- гидроцефальный (при обструктивной или нормотензивной гидроцефалии);
- сосудистый:[4]
- двусторонние инфаркты в области базальных ганглиев и/или лобных долей;
- односторонний инфаркт или кровоизлияние в области базальных ганглиев;
- множественные лакунарные инфаркты;
- диффузное ишемическое поражение белого вещества (болезнь Бинсвангера);
- инфаркт или кровоизлияние в области среднего мозга.
- Паркинсонизм в рамках других дегенеративных заболеваний с поражением экстрапирамидной системы (атипичный паркинсонизм, "паркинсонизм-плюс"):
- множественные системные атрофии (МСА):
- стриатонигральная дегенерация;
- оливопонтоцеребеллярная дегенерация;
- прогрессирующий надъядерный паралич (ПНП) (болезнь Стила—Ричардсона—Ольшевского);
- кортикобазальная дегенерация (КБД);
- болезнь диффузных телец Леви (деменция с тельцами Леви—ДТЛ);
- паркинсонизм—БАС—деменция;
- болезнь Вильсона—Коновалова;
- болезнь Гентингтона (ювенильный вариант Вестфаля);
- болезнь Фара (идиопатическая кальцификация базальных ганглиев);
- нейроакантоцитоз;
- болезнь Крейтцфельдта—Якоба;
- болезнь Мачадо—Джозефа (спиноцеребеллярная атаксия 3-го типа);
- болезнь Галлервордена—Шпатца;
- болезнь Сегавы;
- X-сцепленный синдром «паркинсонизм—дистония» (Lubag);
- паллидарная, паллидонигральная и паллидольюисонитральная дегенерации;
- гемипаркинсонизм—гемиатрофия;
- болезнь Пика (лобно-височная деменция);
- болезнь Альцгеймера;
- другие.
- множественные системные атрофии (МСА):
Этиология[править | править код]
- Основной источник раздела: «Болезни нервной системы»[1]
Происхождение болезни Паркинсона остается до конца не изученным, тем не менее в качестве причины заболевания рассматривается сочетание нескольких факторов:[2][3]
- старение;
- наследственность;
- некоторые токсины и вещества;
- воздействие факторов окружающей среды.[1]
По-видимому, имеет значение комплексное воздействие разнообразных факторов, приводящих в конечном итоге к гибели дофаминергических нейронов черной субстанции по механизму апоптоза или некроза.
Старение[править | править код]
Тот факт, что некоторые проявления Болезнь Паркинсона возникают и при нормальном старении, заставляет предполагать, что одним из причинных факторов паркинсонизма может быть возрастное снижение количества мозговых нейронов.[2][3]
Компенсаторные возможности мозга настолько велики, что симптомы паркинсонизма появляются лишь при потере 80% нейронной массы.[2][3]
Патоморфологически нормальное старение сопровождается уменьшением числа нейронов черной субстанции и наличием в них телец Леви. Старению также сопутствуют нейрохимические изменения в стриатуме — снижение содержания дофамина и фермента тирозингидроксилазы, а также уменьшение числа дофаминовых рецепторов. Однако с помощью позитронно-эмиссионной томографии было доказано, что темпы дегенерации нейронов черной субстанции при болезни Паркинсона в несколько раз выше, чем при нормальном старении.
Наследственность[править | править код]
Примерно 15% лиц с болезнью Паркинсона имеют семейный анамнез этого заболевания, но это необязательно означает, что болезнью Паркинсона является в этих случаях наследственным заболеванием. Возможно, имеет значение воздействие одинаковых факторов внешней среды в популяциях, проживающих в определенном регионе. Описаны семьи с аутосомно-доминантной передачей паркинсонизма и идентифицированы соответствующие патологические гены. Однако эти семейные варианты паркинсонизма фенотипически, генотипически и патоморфологически отличаются как друг от друга, так и от идиопатической болезни Паркинсона. Ген, ответственный за развитие классической болезни Паркинсона, не идентифицирован. Изучение гомозиготных пар близнецов, страдающих паркинсонизмом, показало, что генетические факторы не являются решающими в его развитии. В то же время данные исследований с использованием позитронно-эмиссионной томографии, выявляющих субклиническое нарушение функции дофаминергических нейронов, показали высокую конкордантность этой дисфункции у монозиготных близнецов, что может свидетельствовать о возможности наследования предрасположенности к развитию болезни Паркинсона.
Факторы внешней среды[править | править код]
Наиболее важным фактором окружающей среды, способным вызвать синдром, клинически неотличимый от болезни Паркинсона, считается 1-метил-4-фенил-1,2,3,6-тетрагидропиридин (МФТП). МФТП конвертируется в токсический метаболит — ион 1-метил-1-фенилпиридина (МФП+) под воздействием моноаминоксидазы типа Б (МАО-Б). МФП+ аккумулируется в мито-хондриях, ингибирует фермент дыхательной цепи НАДФ-гидроксилазу и вызывает поражение, а затем гибель нейронов.
Большую роль в патогенезе болезни Паркинсона играет железо. Оно находится в большом количестве в пигментирован¬ных нейронах компактной зоны черной субстанции. При этом преобладает содержание ионов Fe3+ над Fe2+. Ионы Fe3+ наиболее токсичны, так как способствуют образованию свободных радикалов и запускают процесс окислительного стресса, приводящего к гибели клеток. Считается, что практически такую же роль играет алюминий. Тем не менее значение патогенети¬ческой и этиологической роли этих металлов нуждается в уточнении. Возможно, этиологическую роль играют другие, пока не идентифицированные токсины.
Токсины и другие вещества[править | править код]
В 1977 году было описано несколько случаев тяжелого паркинсонизма у молодых наркоманов, принимавших синтетический героин. Этот факт свидетельствует о том, что различные химические вещества могут «запускать» патологический процесс в нейронах головного мозга и вызывать проявления паркинсонизма.[2][3]
Другие причины болезни Паркинсона[править | править код]
Источник раздела: «Болезнь Паркинсона»,[2] «Morbus Parkinson и ее лечение»[3]
- вирусные инфекции, приводящие к постэнцефалитическому паркинсонизму;
- атеросклероз сосудов головного мозга;
- тяжелые и повторные черепно-мозговые травмы.
Длительный прием некоторых препаратов, блокирующих высвобождение или передачу дофамина (например нейролептиков, резерпин содержащих средств), может также привести к появлению симптомов паркинсонизма, поэтому всегда следует уточнить, какую терапию получал больной до установления диагноза Болезнь Паркинсона.
Патоморфология[править | править код]
В 1919 г. К.Н.Третьяков на основании морфологических исследований предположил, что причиной паркинсонизма является поражение черной субстанции. Это гипотеза затем была многократно подтверждена другими исследователями.
Наиболее грубые нарушения выявляются в области компактной зоны черной субстанции. Потеря нейронов начинается и наиболее выражена в вентролатеральном ее отделе в отличие от процессов нормального старения, когда больше страдает дорсальный отдел. Дегенерация также обнаруживается в голубом пятне и прилегающих соседних областях покрышки ствола мозга. В этих зонах отмечается уменьшение количества пигментных нейронов и разрастание глиальных элементов. Многие из еще не погибших нейронов депигментированы, не содержат меланина. Особенно наглядно это заметно при односторонней локализации процесса.
Потеря пигментных нейронов в указанных областях приводит к нарушению связей компактной зоны черной субстанции со скорлупой и в несколько меньшей степени с хвостатым ядром. Поражаются также дофаминовые пути, идущие от области покрышки к вентральным отделам стриатума, некоторым областям коры большого мозга и, возможно, к спинному мозгу. Страдают норадренергические пути, следующие из голубого пятна к коре большого мозга и другим его отделам. В симпатических ганглиях также обнаруживаются тельца Леви и дегенерация нейронов.
На поздних стадиях заболевания у части больных появляются признаки деменции, что, согласно последним данным, связывают с развитием патологических изменений в области ядра Мейнерта, приводящих к нарушениям корковых ацетилхолиновых проекций. Нередко наблюдается и атрофия коры мозга.
В структурах, в наибольшей степени подвергающихся поражению у больных паркинсонизмом, кроме гибели нейронов и депигментации, встречаются своеобразные клеточные включения, получившие название телец Леви. Как правило, эти включения обнаруживаются именно в тех частях мозга, где отмечается большая концентрация моноаминов (дофамин, норадреналин, серотонин). В последние годы было показано, что при использовании иммуногистохимических методов тельца Леви при болезни Паркинсона всегда обнаруживаются не только в пигментных подкорковых образованиях, но и в коре большого мозга. Электронно-микроскопические исследования телец Леви не дали определенного ответа на вопрос о сущности этих включений. Предполагают, что они содержат сфингомиелин и являются результатом дегенерации нейрофибрилл. Тельца Леви могут встречаться и при других нейродегенеративных заболеваниях, поэтому в настоящее время не считаются специфическим гистологическим маркером болезни Паркинсона. Недавно в черной субстанции и голубом пятне пациентов с болезнью Паркинсона были обнаружены «бледные тельца» — внутриклеточные гранулярные включения, замещающие распадающийся меланин. Возможно, они являются предшественниками телец Леви. Ни при одном другом нейродегенеративном заболевании «бледные тельца» пока не обнаружены.
Патогенез[править | править код]
Основу всех форм паркинсонизма составляет резкое уменьшение количества дофамина в черной субстанции и полосатом теле. В норме количество дофамина в этих образованиях в сотни раз превышает концентрацию дофамина в других структурах мозга, что с несомненностью указывает на его важную роль в деятельности экстрапирамидной системы. Синтез дофамина происходит в телах дофаминергических нейронов, располагающихся в черной субстанции. Здесь он образуется в виде небольших пузырьков—гранул, которые по аксонам нигростриарных нейронов транспортируются к окончаниям аксонов в хвостатом ядре и скапливаются перед синаптической мембраной. Под влиянием приходящих нервных импульсов происходит выход квантов медиатора в синаптическую щель. Высвобождающийся дофамин оказывает воздействие на дофаминергические рецепторы постсинаптической мембраны и вызывает состоянии ее деполя¬ризации. На активацию постсинаптической мембраны используется лишь часть выделившегося медиатора. Предполагается, что около 80% дофамина поглощается обратно в пресинаптическое пространство или инактивируется при помощи фермента КОМТ (катехол-О-метилтрансферазы) или МАО-Б. Все процессы образования и транспортировки дофамина регулируются при помощи механизмов обратной связи через рецепторы пресинаптической мембраны.
Разрушение черной субстанции в экспериментах на животных неизменно сопровождается снижением концентрации дофамина в полосатом теле. Аналогичное явление отмечается у больных паркинсонизмом. Также заметно уменьшается концентрация метаболитов дофамина: гомованилиновой кислоты и активность тирозин-гидроксилазы и дофамин-гидроксилазы — ферментов, необходимых для превращения тирозина в ДОФА и ДОФА в дофамин. Эти биохимические нарушения являются результатом разрушения дофаминовых нейронов и нигростриарных связей. Нарушение обмена норадреналина и серотонина при болезни Паркинсона менее выражены, что свидетельствует о меньшей степени поражения адренергических и серотонинергических нейронов, располагающихся в голубом пятне и ядрах средней линии по сравнению с нигральными дофаминергическими нейронами.
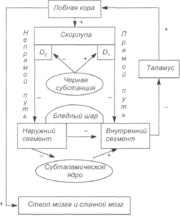
Дисфунция дофаминергической системы вызывает нарушения взаимодействия полосатого тела с другими базальными ганглиями и корой мозга. Базальные ганглии связаны между собой и корой большого мозга посредством нейрональных кругов, которые соединяют пре- и постцентральные сенсомоторные области, базальные ганглии, передневентральный и вентролатеральный отделы таламуса. Выделяются два основных круга (пути) — прямой и непрямой (схема 1).
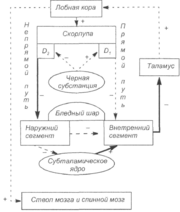
Прямой путь соединяет скорлупу и внутренний сегмент бледного шара; непрямой проходит через наружный сегмент бледного шара, субталамическое ядро и далее к внутреннему сегменту бледного шара. Субталамическое ядро оказывает активирующее влияние на внутренний сегмент бледного шара, в то время как все остальные связи базальных ганглиев, включая их связь с таламусом, являются тормозными (ГАМК-ергическими). Прямой путь, преимущественно регулируется D1-дофаминовыми рецепторами, а непрямой — D2-рецепторами. Дофаминергические влияния нигростриарных нейронов облегчают передачу импульсов в прямом пути (путем стимуляции D1-peцепторов) и подавляют в непрямом (путем стимуляции D2-рецепторов). В результате дофамин уменьшает ингибирующее влияние базальных ганглиев, что ведет к облегчению таламокортикальной передачи и «растормаживанию» моторной коры. Вследствие этого становится возможна передача двигательной программы от премоторной коры к исполнительной прецентральной извилине. Патофизиологической основой паркинсонизма является чрезмерная тормозная активность базальных ганглиев, возникающая вследствие их дофаминергической денервации, что приводит к подавлению двигательных отделов коры и развитию акинезии (схема 2). При гиперкинезах наблюдаются обратная связь (схема 3).
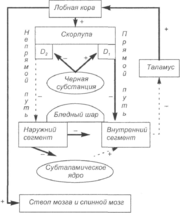
Развитию этих нарушений противостоят значительные компенсаторные механизмы. Известно, что у больных паркинсонизмом отмечается увеличение соотношения гомованилиновая кислота/дофамин, что свидетельствует о том, что оставшиеся нейроны работают более активно, чем у здорового человека. Это явление расценивается как компенсаторный механизм, предохраняющий от раннего появления симптомов заболевания. Экспериментально было показано, что уровень дофамина в полосатом теле может снизиться до 20 % от нормы, прежде чем возникнут клинические проявления заболевания. Повышение чувствительности дофаминовых постсинаптических рецепторов также может служить компенсаторным механизмом, тормозящим развитие паркинсонизма. Развитие клинических проявлений заболевания происходит, когда все возможности компенсации недостатка дофаминовой системы будут исчерпаны.
Кроме дофамина, в хвостатом ядре обнаружена значительная концентрация другого медиатора ЦНС — ацетилхолина. Предполагается, что ацетилхолин образуется в многочисленных вставочных нейронах полосатого тела, а не попадает туда, подобно дофамину, из других отделов мозга. Как уже указывалось выше, дофамин тормозит активность хвостатого ядра, тогда как ацетилхолин является облегчающим медиатором, способствующим возбуждению каудальных нейронов. В результате функциональное состояние хвостатого ядра определяется балансом между дофаминергическими и ацетилхолинергическими системами с относительным преобладанием последних. В то же время в лобных долях определяется дефицит ацетилхолина, что, возможно, является одной из причин когнитивных и поведенческих нарушений при болезни Паркинсона.
Исследования взаимоотношений между черной субстанцией и полосатым телом показали, что они имеют двусторонний характер и работают по принципу обратной связи. Воздействие хвостатого ядра на черную субстанцию происходит при помощи ГАМК, а также других нейротрансмиттеров. Стриарные ГАМК-ергические нейроны, оказывая тормозное воздействие на активность дофаминергических нейронов черной субстанции, тем самым контролируют уровень дофамина в полосатом теле. Хвостатое ядро, кроме тормозных влияний, может оказывать на черную субстанцию и возбуждающее влияние при помощи субстанции P. Нейроны, содержащие этот медиатор, проецируются из хвостатого ядра в черную субстанцию. Таким образом, нигростриарные связи являются сложной функциональной системой, далеко не однородной по своим физиологическим и биохимическим компонентам. И самые разнообразные нарушения в этой системе и окружающих ее образованиях приводят к развитию основных клинических симптомов паркинсонизма.
Клиника[править | править код]
Основными проявлениями паркинсонизма служат гипокинезия, мышечная ригидность, тремор и постуральные расстройства.
Гипокинезия[править | править код]
Гипокинезия — трудность инициации произвольных, спонтанных и автоматизированных движений. При попытке начать движение предназначенные для этого мышцы-агонисты сокращаются недостаточно, в результате движение получается чересчур медленным и не достигает конечной цели. Одним из признаков гипокинезии является брадикинезия. Под брадикинезией понимают замедление движений с прогрессивным уменьшением амплитуды при их повторном выполнении. Первыми проявлениями гипокинезии могут быть затруднение и неловкость мелких движений пальцев — застегивание пуговиц, завязывание шнурков, письмо. Гипокинезия выражается также в уменьшении амплитуды физиологической синкинезии — качания рук при ходьбе (ахейрокинез), в укорочении шага, в обеднении мимических движений (гипомимия). Лицо становится маскообразным, выражая иногда застывшую гримасу удивления или печали, что может быть связано с некоторым расширением глазных щелей. Значительно урежаются мигательные движения век, речь становится монотонной и невнятной. При гипокинезии особенно затрудняется одновременное выполнение различных движений, а также комплексных движений. Все эти признаки могут быть замечены при внимательном осмотре больного, хотя вначале они бывают выражены незначительно, часто только на одной половине тела (гемипаркинсонизм) и/или в дистальных группах мышц. Впоследствии они вовлекают множество мышечных групп билатерально. Гипокинезия является наиболее инвалидизирующим признаком болезни Паркинсона.
Для выявления гипокинезии в дебюте болезни Паркинсона требуется проведение определенных проб: ритмичное быстрое постукивание большим и указательным пальцами, постукивание ногой по полу, сжимание-разжимание кулаков, пронация-супинация рук, изучение почерка пациента (обнаружение микрографии). Особенно тяжелым проявлением акинезии является так называемый феномен «застывания» — резкое и неожиданное полное прекращение двигательной активности. Больные могут длительное время поддерживать позы, невозможные для здоровых людей, например лежать, держа голову над подушкой (симптом «воздушной подушки»). Чаще всего «застывания» возникают при попытке встать со стула, начать ходьбу, повернуться или пройти через узкое пространство — дверной проем, коридор. Остановиться больному порой бывает так же трудно, как и начать движение. Изредка наблюдается феномен «парадоксальной кинезии»: больной, с трудом поднимающийся со стула, может легко взбегать по лестнице, ходить, переступая через небольшие препятствия, танцевать. Временное "растормаживание" возникает под влиянием аффекта радости или страха. При идиопатической болезни Паркинсона феномен «застывания» обычно наблюдается на продвинутых стадиях и, возможно, является осложнением длительной терапии дофаминергическими препаратами. При других нейродегенеративных заболеваниях (прогрессирующий надъядерный паралич) феномен «застывания», преимущественно в виде нарушения инициации ходьбы, может иметь место уже в самом начале болезни.
Патофизиологические механизмы гипокинезии остаются до конца невыясненными. Предполагается, что возникновение гипокинезии является результатом нарушения связей между базальными ганглиями, премоторной и моторной корой.
Ригидность[править | править код]
Ригидность — повышение тонуса мышц, которое ощущается во время пассивных движений в суставе, обусловленное одновременным сокращением мышц агонистов и антагонистов. Ригидность часто бывает асимметричной, особенно в начале заболевания. Она наиболее выражена в сгибателях конечностей и аксиальных мышцах. Степень ригидности может варьировать на протяжении дня, она может увеличиваться при стрессах и уменьшаться после сна и отдыха. Ригидность мышц часто бывает причиной болей в спине и в плечевом суставе у пациентов с болезнью Паркинсона. Такие болевые синдромы могут быть первыми признаками паркинсонизма и нередко приводят к неправильным диагнозам. Для более точной оценки ригидности и выявления асимметрии, которая при обычном исследовании незаметна, можно прибегнуть к специальным приемам — попросить пациента производить движения контралатеральной рукой или сжать ее в кулак. При этом тонус на исследуемой стороне увеличивается. При ригидности мышц во время пассивного движения исследующий ощущает одинаковое сопротивление на всем протяжении движения как при сгибании, так и при разгибании (симптом «свинцовой трубки»). Степень сопротивления в отличие от спастичности практически не зависит от скорости движения или от прилагаемой силы. Если при исследовании ригидности отмечается периодическое увеличение сопротивления, создающее впечатление соскакивания зацепляющихся между собой зубьев шестерен, говорят о феномене «зубчатого колеса». Последний обусловлен наслаивающимся на ригидность тремором. По мере прогрессирования заболевания ригидность постепенно нарастает, что сопровождается развитием характерной позы с функциональным доминированием сгибателей: голова согнута и наклонена вперед, руки согнуты в локтевых суставах и приведены к туловищу, спина согнута, ноги слегка согнуты в тазобедренных и коленных суставах.
Патофизиологические механизмы ригидности также не совсем ясны. Существует предположение, что мышечные веретена при паркинсонизме имеют повышенную чувствительность, обусловленную чрезмерной активностью гамма-мотонейронов. Многочисленными клинико-экспериментальными исследованиями установлено, что при паркинсонизме остается неизменным фазический компонент рефлекса на растяжение, тогда как тонический его компонент заметно усиливается. Кроме того, было показано, что у больных паркинсонизмом усиливается так называемый длиннолатентный рефлекс на растяжение, дуга которого проходит через головной мозг. Вероятно предположение, что ригидность является результатом повышенной активности механизмов длиннолатентного и тонического рефлексов на растяжение, освобожденных из-под контроля базальных ганглиев.
Тремор покоя[править | править код]
Тремор покоя — типичный симптом идиопатической болезни Паркинсона. При других паркинсонических синдромах тремор либо отсутствует совсем, либо носит характер постурального или кинетического тремора. Амплитуда тремора увеличивается при умственной нагрузке, стрессе, при движении конечностями, не вовлеченными в тремор (например, амплитуда тремора в руках усиливается при ходьбе), и уменьшается при произвольном движении той конечности, которая вовлечена в тремор. Во время сна паркинсонический тремор исчезает. Частота типичного тремора покоя составляет 4—8 Гц. Частота дрожания в разных частях тела может быть различной, что свидетельствует об отсутствии единого генератора паркинсонического ритма. Он варьирует по интенсивности в течение дня, исчезая во время сна. Примерно у 75 % больных с БП тремор является первым проявлением болезни и может быть легко замечен при осмотре пациента. Наиболее типичны ритмичные движения большого пальца кисти по направлению к остальным, напоминающие счет монет или скатывание пилюль. Иногда больные жалуются на ощущение дрожания внутри себя. Тремор начинается обычно в дистальной части одной конечности (чаще в руке) и очень редко в ноге. В ногах тремор покоя проявляется, когда больной лежит или сидит, но, как правило, исчезает в положении стоя и во время ходьбы. По мере прогрессирования болезни тремор распространяется на проксимальные отделы руки, затем на ипсилатеральную ногу и на контралатеральную руку. Позднее возможно вовлечение подбородка или губ. Выраженность тремора может уменьшаться при значительном повышение ригидности на поздних стадиях заболевания вплоть до полного его исчезновения. У 30 — 60 % с болезнью Паркинсона наряду с тремором покоя может выявляться постуральный и кинетический тремор. В патогенезе тремора ведущая роль отводится группе вентролатеральных ядер таламуса, главным образом промежуточному вентральному ядру, получающему афферентацию от спиноталамического пути и мозжечка. Нейроны промежуточного вентрального ядра обладают свойством самогенерации ритмической активности с частотой 4—6 Гц; кроме того, их функция подавляется во время сна и произвольных движений. Треморогенные импульсы передаются из таламуса к премоторной и моторной коре и далее по пирамидному пути к периферическим мотонейронам. Кроме того, предполагается, что ритмическая активность нейронов таламуса поддерживается благодаря афферентному потоку из мышц, вовлеченных в тремор. Таким образом формируется сложная самоподдерживающаяся система, в которой участвуют структуры различных уровней нервной системы.
Постуральная неустойчивость[править | править код]
Постуральная неустойчивость — снижение или отсутствие способности поддержания положения центра тяжести тела, что в комбинации с акинезией и ригидностью приводит к нарушению ходьбы и падениям. Постуральная неустойчивость, как правило, развивается через несколько лет от начала заболевания и становится инвалидизирующей на поздних стадиях болезни. Вследствие выраженной гипокинезии затрудняется инициация и смена движений. Когда больной начинает ходьбу или хочет изменить ее направление, возникает впечатление, что он начинает топтаться на месте, все более наклоняясь вперед. На самом деле он пытается «догнать» центр тяжести тела мелкими семенящими шагами (пропульсия). Нередко это может закончиться падением, при этом больные не способны предупредить ушибы, так как защитная реакция — упор на руки — у них не успевает срабатывать. Несмотря на неустойчивость, больные не расставляют широко ноги при ходьбе, как это бывает при мозжечковой атаксии.
Для исследовании постуральной устойчивости пациента просят стоять, соединив стопы вместе, а стоящий за спиной больного врач неожиданно, но несильно, тянет его за плечи назад. Пациенты с нарушенными постуральными рефлексами сделают более чем два шага назад для того, чтобы удержаться в вертикальном положении (ретропульсия). При более грубых нарушениях больной может упасть. Нарушения равновесия определяются замедленностью и неадекватностью предупреждающих постуральных реакций при болезни Паркинсона. Предполагается, что патогенез этих расстройств обусловлен нарушением модулирующих влияний бледного шара на области премоторной коры, тесно связанные с подготовкой и координацией движения.
Нарушения сна[править | править код]
У большинства больных с болезнью Паркинсона наблюдаются нарушения сна в виде затрудненного засыпания, уменьшения длительности сна и его фазы с быстрыми движениями глаз. Расстройства сна отчасти связаны с ночной акинезией — трудностью поворотов во сне. Такие пациенты также жалуются на частые ночные пробуждения, после которых они долго не могут заснуть. Нарушения сна могут быть связаны также с препаратами леводопы, если больной их принимает меньше чем за 30 мин до отхода ко сну. Длительный прием препаратов леводопы может быть причиной ярких сновидений. Последнее может предшествовать развитию дофаминового психоза. Жалобы больного на плохой сон и раннее утреннее пробуждение могут быть проявлением депрессии.
Психические расстройства[править | править код]
При длительном лечении препаратами леводопы или агонистами дофаминовых рецепторов у 10—30% больных развивается спутанность сознания, иллюзии и галлюцинации. Предполагается, что в основе этих расстройств лежит гиперчувствительность лимбических постсинаптических дофаминовых рецепторов к противопаркинсоническим препаратам, которая возникает вследствие уменьшения центральной дофаминергической активности. Вероятность развития психоза тем больше, чем больше длительность болезни и лечения. Факторами риска для развития спутанности и «поздних галлюцинаций» на продвинутых стадиях является сопутствующая деменция и прием антпихолинергических препаратов. Вначале у больных возникают зрительные иллюзии или псевдогаллюцинации (т. е. больной сохраняет критику к галлюцинациям), впоследствии же могут появиться истинные галлюцинации (с отсутствием критики) или паранойяльный психоз. Психотические эпизоды иногда возникают также после оперативного вмешательства под местной анестезией или общим наркозом. Следует иметь в виду, что галлюцинаторный синдром сопутствует или может возникать при назначении препаратов леводопы у больных с деменцией с тельцами Леви.
Депрессия[править | править код]
У пациентов с болезнью Паркинсона часто возникают психические расстройства, такие, как когнитивные нарушения вплоть до деменции, депрессия, состояние спутанности и психозы. Они могут быть связаны с самой болезнью, индуцироваться противопаркинсоническими препаратами или быть проявлением сопутствующего психического заболевания.
Депрессия легкой или средней степени встречается у большей части больных с болезнью Паркинсона. Возможно, в части случаев она носит реактивный характер в ответ на тяжелый двигательный дефект. С другой стороны, имеется много свидетельств в пользу того, что депрессия при болезни Паркинсона является результатом органического поражения мозга. Нередко депрессия имеет место у больных с начальными стадиями болезни, иногда она предшествует проявлению двигательного дефекта и может сохраняться на фоне успешной терапевтической коррекции двигательных расстройств. Навязчивость («акайрия»), в прошлом считавшаяся неотъемлемой чертой болезни Паркинсона, реально встречается не так уж часто.
Деменция[править | править код]
Деменция встречается примерно у 10—25 % больных на поздних стадиях болезни. Более легкие когнитивные нарушения, не достигающие степени деменции, встречаются чаще. Возможно, что сопутствующая сенильная деменция альцгеймеровского типа является причиной более высокой частоты деменции в пожилой популяции больных болезнью Паркинсона, по сравнению с более молодыми. Другой формой, при которой характерно сочетание синдрома паркинсонизма и слабоумия, является деменция с тельцами Леви, которая может быть спутана с болезнью Альцгеймера. Деменция может проявляться или усугубляться при приеме ангихолинергических средств или в случае сопутствующей депрессии. Причиной деменции при болезни Паркинсона считается дисфункция лобной доли и полосатого тела, что проявляется нарушением памяти в отсутствие первичной афазии, апраксии и агнозий (так называемая подкорковая деменция). Быстро развивающаяся тяжелая деменция, которая выступает на первый план в клинической картине, атипичный паттерн нейропсихологических расстройств должны ставить под сомнение диагноз болезни Паркинсона и заставить думать о болезни Альцгеймера, прогрессирующем надъядерном параличе, деменции с тельцами Леви или субкортикальной артериосклеротической энцефалопатии Бинсвангера.
Другие симптомы[править | править код]
Довольно часто у больных возникают расстройства конвергенции и аккомодации, реже — блефароспазм.
У большинства больных отмечается нарушение вегетативных функций: гиперсаливация, сальность кожи лица, повышение потливости или, наоборот, сухость кожи, задержка мочеиспускания. Больные часто жалуются на запоры, обусловленные атонией толстой кишки. Могут возникать вегетативные кризы, сопровождающиеся резкой гиперемией лица, повышенной потливостью, тахикардией, эмоциональным напряжением, страхом.
Боль, жжение, похолодание, онемение и другие сенсорные симптомы наблюдаются почти у половины пациентов с болезнью Паркинсона и часто служат поводом для ошибочной диагностики суставно-мышечных или иных заболеваний.
Формы заболевания[править | править код]
Соотношение выраженности основных симптомов заболевания у разных больных может значительно колебаться. В связи с этим различают следующие формы заболевания:
- акинетико-ригидную,
- ригидно-дрожательную
- и дрожательную.
Определение формы заболевания является весьма существенным фактором при выборе метода лечения.
Диагноз и дифференциальный диагноз[править | править код]
Диагноз паркинсонизма обычно не представляет трудностей. Однако могут иметь место случаи, когда необходимо проводить дифференциальный диагноз с некоторыми состояниями, имеющими внешне схожие проявления (псевдопаркинсонизм):
- психомоторная заторможенность (депрессия, кататонический ступор, истерия, гиперсомния);
- мышечный гипертонус (нейромиотония, синдром «ригидного человека»);
- апраксия ходьбы (лакунарное состояние, нормотензивная гидроцефалия, опухоли мозга, другие дегенеративные заболевания);
- эссенциальный и другие формы тремора,
- ряд иных состояний.
Тщательное клиническое исследование и при необходимости применение инструментальных и лабораторных методов исследования, как правило, позволяют достаточно надежно проводить дифференциальный диагноз.
Для диагностики синдрома паркинсонизма необходимо наличие у пациента гипокинезии и одного или нескольких следующих симптомов:
- тремор покоя,
- ригидность,
- постуральные нарушения.
Помимо болезни Паркинсона, остальные случаи паркиснонизма представлены двумя группами заболеваний. Первая группа — это заболевания, связанные с поражением нигростриарной системы вполне определенной этиологии — вторичный (симптоматический) паркинсонизм, составляющий около 8% случаев. К этой группе относят токсический паркинсонизм, лекарственный, постэнцефалитический, сосудистый, посттравматический, а также паркинсонизм вследствие внутричерепных объемных образований.
Вторая группа заболеваний, при которых может наблюдаться синдром паркинсонизма — это мультисистемные дегенерации спорадические и наследственные, составляющие около 12% случаев. Поскольку паркинсонизм при этих заболеваниях не всегда является ведущим и облигатным признаком и обычно сочетается с симптомами поражения других отделов нервной системы, для обозначения группы подобных нозологии используется термин «паркинсонизм-плюс». К дегенеративным заболеваниям, при которых наблюдается синдром паркинсонизма, относятся мультисистемная атрофия, прогрессирующий надъядерный паралич, синдром паркинсонизм-БАС-деменция, кортикобазальная дегенерация, деменция с тельцами Леви, болезнь Геллервордена-Шпатца, болезнь Вильсона-Коновалова, ювенильная форма хореи Гентингтона и некоторые другие редкие заболевания.
В 1992 г. Huges предложил критерии клинической диагностики БП, позволяющие установить диагноз с точностью до 93% (согласно данным аутопсий):
- наличие гипокинезии и как минимум одного из следующих симптомов: ригидность, тремор покоя 4—6 Гц, постуральные нарушения;
- стойкий положительный эффект леводопы;
- асимметричный дебют заболевания (стадия гемипаркинсонизма);
- прогрессирующее течение;
- отсутствие в анамнезе возможных этиологических факторов вторичного паркинсонизма (прием нейролептиков, достоверно перенесенный энцефалит, острые нарушения мозгового кровообращения, повторные или тяжелые черепно-мозговые травмы);
- отсутствие следующих симптомов:
- на всех стадиях заболевания:
- отчетливой мозжечковой и/или пирамидной симптоматики,
- надъядерного паралича взора,
- окулогирных кризов,
- на ранних стадиях заболевания:
- грубых постуральных расстройств,
- грубой прогрессирующей вегетативной недостаточности,
- грубой деменции.
- на всех стадиях заболевания:
Эти критерии должны соблюдаться лишь при отборе пациентов для научных исследований. Для предварительного диагноза в практической работе достаточно выполнение лишь первых двух пунктов.
Инструментальные исследования, включая МРТ, не могут подтвердить диагноз болезни Паркинсона и проводятся лишь для исключения других заболеваний, перечисленных выше. Лишь позитронно-эмиссионная томография позволяет подтвердить диагноз, даже на доклинической стадии, путем выявления снижения накопления радиоактивного препарата флуородопы в полосатом теле.
Лечение[править | править код]
- Основная статья: Лечение болезни Паркинсона
Примечания[править | править код]
- ↑ 1,0 1,1 1,2 Болезни нервной системы. Руководство для врачей. Под ред. Н.Н.Яхно, Д.Р.Штульмана. М.: «Медицина», 2001. Т.2
- ↑ 2,0 2,1 2,2 2,3 2,4 2,5 2,6 Болезнь Паркинсона — Клиника нервных болезней им. М.И.Аствацатурова. Военно-Медицинская академия им. С.М.Кирова
- ↑ 3,0 3,1 3,2 3,3 3,4 3,5 3,6 Ф.Хоффманн — Ля Рош Лтд. (Базель, Швейцария). «Morbus Parkinson и ее лечение». Москва, 2000.
- ↑ Диагностика сосудистого паркинсонизма требует установления причинно-следственных связей между сосудистым повреждением мозга, верифицированным путем нейровизуализации, и паркинсонизмом.
Нервная система : ЦНС • Нервная ткань • Нейрон • Нейроглия • Гемато-энцефалический барьер • Сухожильный рефлекс • Экстрапирамидная система
Синдромы — Болевые синдромы • Экстрапирамидные гиперкинетические синдромы • Нарушения сна • Синдром хронической усталости
Заболевания — Черепно‐мозговая травма (Патофизиология черепно-мозговой травмы) • Паркинсонизм (Болезнь Паркинсона • Лечение болезни Паркинсона) • Арахноидит