Вода
- Основной источник статьи: Большая российская энциклопедия[1]
ВОДА́ (оксид водорода), простейшее устойчивое химическое соединение водорода с кислородом, H2O; при нормальных условиях – жидкость без запаха, вкуса и цвета. Одно из самых распространённых на Земле соединений, играющее исключительно важную роль в разнообразных процессах живой и неживой природы Земли. Истинный состав воды как сложного вещества был впервые установлен А. Лавуазье в 1783. Греческое название ὕδωρ (см. Гидро…), лат. aqua – аква.
Вода как вещество
Распространённость в природе
Вода образует гидросферу, входит в связанном виде в состав различных минералов и горных пород, является обязательным компонентом всех живых организмов, присутствует в почве и атмосфере. Молекулы воды обнаружены в межзвёздном пространстве; вода входит в состав комет, большинства планет Солнечной системы, спутников.
Количество воды на поверхности Земли оценивается в 1,39·1021 кг, бóльшая часть содержится в морях и океанах (1,34·1021 кг); см. также таблицу в статье Воды суши. В глубинных слоях Земли воды значительно больше, чем на поверхности, – (1,1–1,3)·1021 кг в литосфере, (1,3–1,5)·1022 кг в мантии Земли. Количество доступных пресных вод составляет 2·1017 кг. В атмосфере находится около 1,3·1016 кг. На Земле существует постоянный кругооборот воды (см. Влагооборот, Водный баланс).
Природная вода всегда содержит растворённые соли, газы и органические вещества, а также коллоидные частицы и микроорганизмы. Состав примесей зависит от происхождения воды. По минерализации различают следующие виды воды: атмосферные осадки (10–20 мг/кг), ультрапресные (до 200 мг/кг), пресные (200–500 мг/кг), слабоминерализованные (0,5–1,0 г/кг), солоноватые (1–3 г/кг), солёные (3–10 г/кг), с повышенной солёностью (10–35 г/кг), переходные к рассолам (35–50 г/кг), рассолы (более 50 мг/кг); максимальная концентрации солей содержат воды соляных озёр (до 300 г/кг) и глубокозалегающие подземные воды (до 600 г/кг). В пресных водах преобладают ионы HCO3–, Ca2+, Mg2+, Cl–, Na+, SO42–, K+, (см. также Минеральные воды, Жёсткость воды). К микрокомпонентам природной воды относятся бор, литий, рубидий, медь, цинк, алюминий, бериллий, вольфрам, уран, бром, йод и др. Из растворённых газов в природных водах присутствуют азот, кислород, углекислый газ, благородные газы, редко сероводород и углеводороды. Концентрация органических веществ в водах рек около 20 мг/кг, в воде океана – около 4 мг/кг, причём их состав чрезвычайно разнообразен. См. также Гидрохимия.
Изотопный состав
Существует 9 разновидностей молекул В., включающих только стабильные изотопы. Их содержание в природной В. в среднем составляет (мол. %):
1H216O — 99,73;
1H218O — 0,2;
1H217O — 0,04;
1H2H16O — 0,03;
остальные присутствуют в ничтожных количествах. Природная вода содержит также радиоактивный тритий. По физическим свойствам изотопные разновидности воды несколько различаются; тяжёлая вода существенно отличается по свойствам от природной.
Строение молекулы и физические свойства
Атомы H и O в молекуле воды расположены в вершинах равнобедренного треугольника с длиной связи O–H 0,0957 нм; валентный угол H–O–H 104,5°. Электронная плотность молекулы воды распределена таким образом, что возникают 4 полюса зарядов, расположенные в вершинах искажённого тетраэдра: два положительных на атомах H и два отрицательных на неподелённых электронных парах атома O. Дипольный момент 6,17·10–30 Кл·м, энергия ионизации 12,6 эВ, сродство к протону 7,1 эВ.
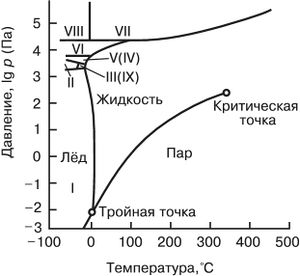
Вода может существовать в твёрдом (лёд), жидком и газообразном состояниях. Дипольные молекулы воды взаимодействуют друг с другом и с полярными молекулами других веществ (атомы водорода могут образовывать водородные связи с атомами кислорода, азота, фтора, хлора, серы и др.). Каждая молекула воды способна образовывать 4 водородные связи: две – как донор протонов, две – как акцептор. Средняя длина таких связей в кристаллических модификациях льда (известно 10 кристаллических модификаций льда) и кристаллогидратах около 0,28 нм. Угол O–HO стремится к 180°. В обычных условиях лёд существует в гексагональной модификации; угол H–O–H близок к тетраэдрическому (109,5°), что обусловливает рыхлость структуры льда. При увеличении внешнего давления лёд переходит в модификации с большей плотностью (рисунок); максимальная плотность льда 1660 кг/м3.
Трёхмерная сетка водородных связей, построенная из тетраэдров, сохраняется и в жидкой воде. Установлено объединение молекул воды в ассоциаты и даже в обширные кластеры (130 молекул H2O при 0 °C, 90 – при 20 °C, 60 – при 72 °C, время жизни 10–11–10–10 с).
Некоторые параметры, характеризующие основные физические свойства воды в различных агрегатных состояниях (при давлении 1013,25 гПа), приведены далее:
| Температура кипения, °С | 100 |
| Температура плавления, °С | 0 |
| Температура критическая, °С | 374,15 |
| Давление критическое, МПа | 22,06 |
| Плотность критическая, кг/м3 | 322 |
| Теплота плавления, кДж/моль | 5,99 |
| Теплота испарения, кДж/моль при 100 °С | 40,649 |
| Плотность, кг/м3 | |
| лёд (гексагональная структура) при 0 °С | 916,8 |
| жидкость | |
| при 0 °С | 999,87 |
| при 3,98 °С | 1000 |
| при 20 °С | 998,23 |
| при 100 °С | 958,38 |
| Теплопроводность, мВт/(м·К) жидкость | |
| при 0 °С | 561 |
| при 20 °С | 598,5 |
| при 100 °С | 678,8 |
| Удельная электропроводность, Ом-1·м-1 | |
| лёд при 0 °С | 0,4·10-10 |
| жидкость | |
| при 0 °С | 1,47·10-10 |
| при 50 °С | 18,9·10-10 |
| Удельная теплоёмкость, Дж/(кг-К) жидкость | |
| при 0 °С | 4217 |
| при 15 °С | 4168 |
| при 40 °С | 4179 |
| при 100 °С | 4216 |
| Диэлектрическая проницаемость | |
| лёд при 0 °С | 74,6 |
| жидкость при 20 °С | 81 |
| Динамическая вязкость, мПа·с жидкость | |
| при 0 °С | 1,792 |
| при 20 °С | 1,005 |
| при 100 °С | 0,2821 |
| Поверхностное натяжение, мН/м жидкость на границе с воздухом | |
| при 0 °С | 75,65 |
| при 20 °С | 72,74 |
| при 100 °С | 58,92 |